Клітинний банк ліній з тканин людини і тварин
Науковий керівник: Лихова Олександра Олександрівна
Науковий ступінь: к.б.н.
Вчене звання: старший дослідник
Посада: старший науковий співробітник відділу моніторингу пухлинного процесу та дизайну терапії
Тел: +38 (044) 259-70-86, +38(063) 424-81-12
E-mail:cellbankkyiv@gmаil.com











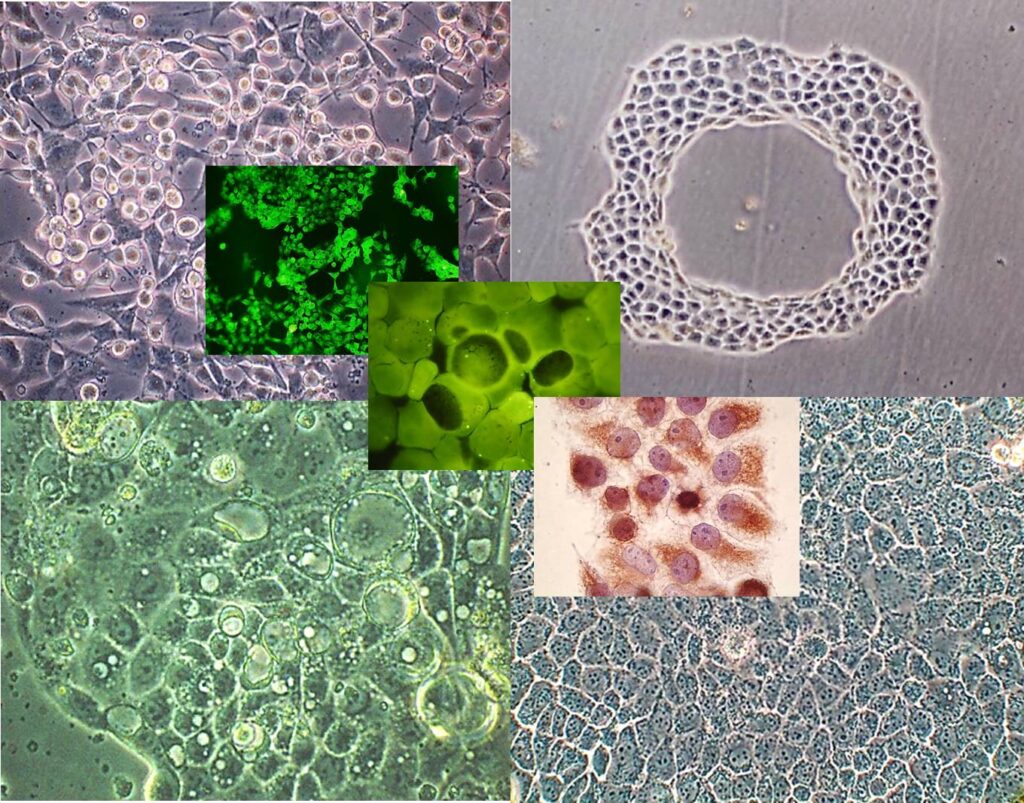
«Клітинний банк ліній з тканин людини та тварин»
Клітинний банк ліній з тканин людини та тварин є найбільш вагомою в Україні офіційною колекцією клітинних матеріалів, призначеною для зібрання, кріозбереження та розповсюдження культур клітин та штамів трансплантованих пухлин. Банк налічує більше 30000 зразків типових та оригінальних ліній клітин з нормальних та пухлинних тканин людини та різних видів тварин — щура, миші, хом’яка, мавпи, свині, собаки, бика, вівці, летючої миші, норки, риби, комах та ін. Колекція клітинних ліній містить більше 200 найменувань, колекція трансплантованих пухлин налічує більше 30 штамів.
Клітинний банк ліній з тканин людини та тварин занесено до Державного реєстру об’єктів, що становлять національне надбання України з 1999 року (Постанова Кабінету Міністрів України №527 від 1.04.1999р.)
Вагому частину наукової роботи Банку складають дослідження біологічних і морфологічних властивостей клітин, їх цитогенетичних та імунофенотипових особливостей. До переліку основних задач Клітинного банку входять також отримання і характеристика нових клітинних ліній з нормальних і пухлинних тканин людини та різних видів тварин.
В роботі Клітинного банку широко застосовуються сучасні методи досліджень: культивування та клонування клітин, трансдукції клітин різними генами, а також імунологічні, вірусологічні, біохімічні, морфологічні та цитогенетичні методи досліджень.
Співробітники Банку мають великий досвід у тестуванні in vitro та in vivo ефективності дії речовин з протипухлинною та антивірусною активністю різної природи (хімічних, фізичних, біологічних) і механізмів дії. У лабораторіях Клітинного банку розроблені модельні клітинні системи для визначення біологічної активності різних цитокінів in vitro(інтерлейкінів, факторів росту, фактору некрозу пухлин, інтерферонів та ін.).
Для проведення вищезазначених досліджень Банк має відповідну офіційну акредитацію.
КАТАЛОГ. БАНК КЛІТИННИХ ЛІНІЙ З ТКАНИН ЛЮДИНИ І ТВАРИН
Клітинний банк ліній з тканин людини та тварин надає високоякісні послуги:
Депонування дослідницьких біологічних матеріалів в умовах рідкого азоту (- 196 о С)
- Приймання на довгострокове зберігання (депонування) у кріобанку клітинних ліній і штамів, вірусів, ДНК, зразків пухлин та ін.дослідницьких матеріалів наукових та учбових установ.
- Кріоконсервація та наступне довгострокове зберігання у кріобанку в умовах рідкого азоту зразків периферичної крові, кордової крові та кісткового мозку людини та інших живих істот.
Депонування біологічних матеріалів від онкологічних хворих
- Зберігання фрагментів пухлин, отриманих під час хірургічного втручання, у рідкому азоті.
- Приготування стерильних фрагментованих суспензій клітин пухлин та програмована їх кріоконсервація і зберігання (у життєздатному стані).
- Отримання суспензій мононуклеарів крові, кісткового мозку від хворих на лейкози та їх програмована кріоконсервація і довгострокове зберігання (у життєздатному стані).
- Зберігання зразків плазми чи сироватки крові або іншої біологічної рідини в умовах скрапленого азоту.
- Забезпечення дослідників штамами пухлин та клітинних ліній.
На базі Клітинного банку ліній з тканин людини та тварин виконуються науково-дослідні проекти:
- Прескринінгові дослідження лікарських засобів та медичних виробів in vitro та ex vivo (з використанням клітинних модельних систем)
- Дослідження токсичності лікарських засобів та медичних виробів на експериментальних тваринах in vivo
- Створення та тестування експериментальних моделей «патологічних станів» in vitro та ex vivo: фіброз, запалення, псоріаз,стеатоз та ін.
- Формування функціональних систем мультиорганної оцінки токсичності речовин ex vivo
Вибрані публікації співробітників Клітинного банку:
- Sarnatskaya V, Shlapa Y, Kolesnik D, Lykhova O, Klymchuk D, Solopan S, Lyubchyk S, Golovynska I, Qu J, Stepanov Y, Belous A. Bioactivity of cerium dioxide nanoparticles as a function of size and surface features. Biomater Sci. – 2024; 12(10):2689-2704. (Q1)
- Kozak T, Lykhova O, Serhiichuk T, Bezdieniezhnykh N, Chekhun V. Optimization of experimental model systems for evaluating reciprocal influence of bifidobacterium animalis and human breast cancer cells in vitro Experimental Oncology. – 2023. – 45(4). – Р. 504–514. (Q4)
- Lykhova O, Zavelevich M, Philchenkov A, Vidasov N, Kozak T, Lozovska Y, Andrusyshyna I, Bishayee A, Borikun T, Lukianova N, Chekhun V. Does insulin make breast cancer cells resistant to doxorubicin toxicity? Naunyn Schmiedebergs Arch Pharmacol. 396(11), 2023, 3111-3122. (Q2)
- Natalia Bezdieniezhnykh, Alexandra Lykhova, Tamara Kozak, Taras Zadvornyi, Tetyana Borikun, Olena Voronina, Natalia Lukianova. Assessment of biosafety and toxicity of hydrophilic gel for implantation in experimental in vitro and in vivo models. BMC Pharmacology and Toxicology. 2022; 23(1): 37. (Q2, Q3)
- Yuliia Shlapa, Serhii Solopan, Veronika Sarnatskaya, Katarina Siposova, Ivana Garcarova, Katerina Veltruska, Illia Timashkov, Oleksandra Lykhova, Denis Kolesnik, Andrey Musatov, Vladimir Nikolaev, Anatolii Belous. Cerium dioxide nanoparticles synthesized via precipitation at constant pH:Synthesis, physical-chemical and antioxidant properties. Colloids and Surfaces B: Biointerfaces. 2022; 220: 112960. (Q1)
- Bezdieniezhnykh N., Holiuk Ye., Gerasymenko S., Saulenko K., Mayko V., Lykhova O. Evaluation of in vitro biocompatibility of scaffolds for the repair of bone defects. Cell and Organ Transplantology. 2021; 9(2): 96-102. (Q4)
- Natalia Bezdieniezhnykh, Aleksandra Lykhova, Hennadii Borschevskyi, Kateryna Dyakun, Ievgen Kruglov. In Vitro Assessment of the Biological Activity of a New Regenerative Agent Prepared From the Concentrate of Deproteinized Dermal Layer of Porcine Skin. EUREKA: Life Sciences. 2020; (6): 12-22.
- Mazurkevych A, Malyuk M, Bezdieniezhnykh N, Starodub L, Kharkevych Y, Jakubczak A and Gryzinska M. Immunophenotypic characteristics and karyotype analysis of bone marrow-derived mesenchymal stem cells of rabbits during in vitro cultivation. Polish Journal of Veterinary Sciences. 2017; 20: 687–69. (Q2)
- N. Bezdieniezhnykh, A. Lykhova, N. Semesiuk, R. Okhrimenko, Yu. Kudryavets. Establishment and characterization of new breast and ovarian cancer cell lines as a model for studying cellular plasticity in vitro. Exp Oncol. 2016; 38 (2): 94–100 (Q4).
- A. Lykhova, Yu.Kudryavets, L.Strokovska, N.Bezdenezhnykh, N.Semesiuk, I.Adamenko, J.Zaharuk, A.Vorontsova. Suppression of proliferation, tumorigenicity and metastasis of lung cancer cells after their transduction by interferon-beta gene in baculovirus vector. Cytokine. 2015; 71(2): 318-26. (Q2)
- N.Bezdenezhnykh, N.Semesiuk, O.Lykhova, V.Zhylchuk, Yu.Kudryavets. Impact of stromal cell components of tumor microenvironments on epithelial-mesenchymal transition in breast cancer cells. Experimental Oncology. 2014; 36(2): 72-78. (Q2)
- A.Lykhova, N.Bezdenezhnykh, N.Semesiuk, I.Adamenko, A. Vorontsova Yu.Kudryavets. Loss of malignancy in mouse melanoma cells by long-term impact of recombinant interferon-beta in vitro is associated with N- and VE-cadherins suppression without inhibition expression of epithelial-mesenchymal transition transcription factors Twist and Slug. J Anal Oncol. 2014; 3(3): 136-145.


